Fenofibrate
Mục lục
1.Thông tin chung
| Tên dược chất | Fenofibrat | Cholin fenofibrat |
| Cấu trúc | 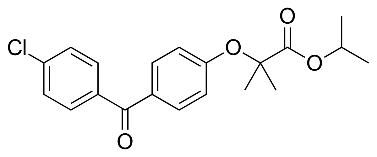 |
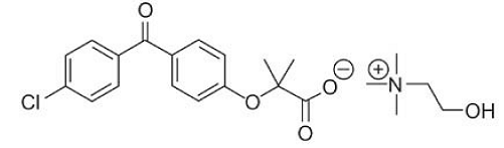 |
| Công thức phân tử | C20H21ClO4 | C22H28ClNO5 |
| KLPT | 360.8 | 421.91 |
| Nhóm tác dụng dược lý | Hạ lipid/cholesterol và triglycerid – ETC | |
TLTK: [1]
2.Biệt dược gốc và các dạng bào chế trên thị trường
2.1.Đơn chất
| STT | Dạng bào chế [2] | Tên biệt dược |
| 1 | Viên nang cứng
(Fenofibrat) |
Tricor
Lipanthyl |
| 2 | Viên nén bao phim
(Fenofibrat) |
Tricor |
| 3 | Viên nang cứng tác dụng kéo dài
(Cholin fenofibrat) |
Trilipix 45mg |
Dạng bào chế phổ biến tại Việt Nam: Viên nang cứng, viên nén bao phim
2.2.Dạng phối hợp:
| STT | Hoạt chất phối hợp [3],[4] | Dạng bào chế | Tên biệt dược |
| 1 | Fenofibrat/ Simvastatin | Viên nén bao phim | Cholib |
| 2 | Fenofibrat/ Pravastatin sodium | Viên nang cứng | Pravafenix |
| 3 | Fenofibrat/ Pitavastatin | Viên nang cứng | Stafen |
| 4 | Atorvastatin calcium | Viên nén | Statix-F |
3.Tính chất lý hóa
| Tên dược chất [1],[5],[6] | Fenofibrat | Cholin fenofibrat |
| Mô tả | Bột màu trắng tới trắng ngà, không mùi. | Bột trắng tới hơi vàng. |
| Tính tan | Thực tế không tan trong nước; hơi tan trong ethanol, methanol; tan được trong aceton, ether, benzen, cloroform. | Tan tự do trong nước |
| Độ tan | Độ tan trong nước: 0.42 mg/L (25°C) | N/A |
| BCS Class | II | N/A |
| Dạng đa hình | Có thể tồn tại ở dạng tinh thể form I, II, III, IV. Trong đó form I là ổn định nhất (dạng được thương mại hóa) [7] | Không có dạng đa hình |
| Nhiệt độ nóng chảy | 79-82oC. | 210oC. |
| Tính hút ẩm | Không hút ẩm | Không hút ẩm |
| pKa | N/A | N/A |
| pH | N/A | N/A |
| Tính chất hóa học | Fenofibrat tương đối trơ về mặt hóa học, nhưng có thể thủy phân trong môi trường kiềm mạnh. | N/A |
| Độ ổn định | Dược chất tương đối bền vững ở những điều kiện bảo quản thông thường. | N/A |
4.Chuyên luận Dược Điển
| Monograph | Dược Điển |
| Fenofibrate | USP, BP, EP |
| Fenofibrate tablets | USP |
| Fenofibrate capsules | USP |
5.Nhà sản xuất API
-
- Everest Organics Limited (India)
- Olon S.p.A (Italy)
- Zhejiang Excel Pharmaceutical Co., Ltd (China)
- Jiangsu Nhwa Pharmaceutical Co., Ltd (China)
- Lee Pharma Limited (India)
- Coprima, S.L. (Spain)
6.Kinh nghiệm đối với hoạt chất – tương ứng với từng dạng bào chế
Chỉ dành cho tài khoản VIP
6.1. Kinh nghiệm thực tế:
-
- Những lưu ý khi xây dựng công thức viên nén bao phim:
- Fenofibrat nóng chảy ở nhiệt độ 79-82oC, nên cần kiểm soát chặt chẽ nhiệt độ sấy cốm.
- Đối với viên nén bao phim hàm lượng 160 mg: Độ hòa tan phụ thuộc nhiều vào kích thước hạt và khả năng rã của viên, nên cần chú ý lựa chọn nguyên liệu với kích thước hạt càng nhỏ càng tốt (tốt nhất < 10 µm) và xây dựng công thức để viên rã nhanh. Do fenofibrat (micronised) thường xốp, tỉ trọng rất nhẹ, nên cần chú ý khi xây dựng cỡ lô ở quy mô công nghiệp, tránh nguy cơ cốm trào ra khi trộn cao tốc hoặc quá đầy máy sấy tầng sôi.
- Đối với viên nén bao phim hàm lượng 145mg: Do thuốc gốc công bố nguyên liệu ở dạng nano, nên thường sẽ phải xây dựng công thức mà nguyên liệu ở dạng nano hoặc quy trình để giảm kích thước nguyên liệu xuống dạng nano (có thể tham khảo quy trình nghiền bi của thuốc gốc).
- Những lưu ý khi xây dựng công thức viên nang cứng:
- Cần chú ý khảo sát nguyên liệu với kích thước hạt phù hợp, tương ứng với mỗi hàm lượng dược chất đóng nang (67mg, 134mg, 200mg, 300mg…).
- Độ hòa tan phụ thuộc nhiều vào kích thước hạt và khả năng rã của viên, nên xây dựng công thức để viên rã nhanh.
- Khi xây dựng công thức và cỡ nang theo thuốc đối chiếu, cần cân nhắc nguy cơ cốm khó đóng vô nang hoặc đóng vô được nhưng viên khó rã do tỉ lệ dược chất trong viên lớn, tỉ trọng nhẹ. Cân nhắc một số biện pháp tăng tỉ trọng của cốm đóng nang (xát hạt ướt, tăng tá dược dính…) nhưng đảm bảo độ rã cho viên (tăng tá dược rã, tăng tá dược độn và đổi cỡ nang…).
6.2. Tài liệu cho xây dựng công thức:
-
-
- Patent số 4895726 (1990) [8]:
- Mô tả phương pháp bào chế viên nang cứng chứa fenofibrat 200mg bằng phương pháp xát hạt ướt.
- Nguyên liệu fenofibrat được giảm kích thước bằng cách trộn cùng natri lauryl sulfat rồi cho qua máy air-jet micronizer. Sau đó fenofibrat được xát hạt ướt và đóng nang.
- Patent số US 7.276,249 B2 (2007) [9][10]
- Mô tả phương pháp bào chế viên nén bao phim fenifibrat 145mg bằng phương pháp tạo hạt tầng sôi.
- Nguyên liệu fenofibrat được nghiền ướt trong máy nghiền bi để giảm kích thước xuống cỡ nanomet. Hỗn dịch nano sau đó được phun lên nhân trơ rồi trộn với các tá dược và dập viên.
-
Tài liệu tham khảo
[1] Pubchem website – Fenofibrate[2] N. Downing, J. Ross, C. Jackevicius, and H. Krumholz, “How Abbott’s fenofibrate franchse avoided generic competition,” Arch Intern Med, vol. 172, no. 9, pp. 724–730, 2012, doi: 10.1001/archinternmed.2012.187.How.
[3] “Full prescribing information of CHOLIB film-coated tablets.” pp. 183–226, [Online].
[4] “Full prescribing information of PRAVAFENIX 40mg/160mg.” [Online].
[5] “Full prescribing information of TRIPILIX capsule, delayed release.” 2021, [Online].
[6] “chemistry review of choline fenofibrate.pdf,” 2008. [Online].
[7] X. Shi, Y. Shao, and X. Sheng, “A new polymorph of fenofibrate prepared by polymer-mediated crystallization,” J. Cryst. Growth, vol. 498, no. May, pp. 93–102, 2018, doi: 10.1016/j.jcrysgro.2018.05.030.
[8] I. B. Curtet, M. Cote, E. Teillaud, and F. Dijon, “Patent No 4895726: Novel dosage form of fenofibrat,” 1990.
[9] S. B. Ruddy, M. J. Wilkins, and C. Cork, “Patent No: US 7276249 B2: Nanoparticulate fibrate formulations,” 2007.
[10] C. Herry, “Patent No US 2011 / 0311619 A1: Pharmaceutical formulation of nanosized fenofibrat,” 2011.

