Forxiga (Dapagliflozin)
 |
 |
| Công ty sở hữu | AstraZeneca Pharmaceuticals | |
| API & liều dùng |
Dapagliflozin (dưới dạng dapaglifozin propanediol monohydrate): 5 mg – 10 mg/ ngày |
|
| Hàm lượng | 5 mg | 10 mg |
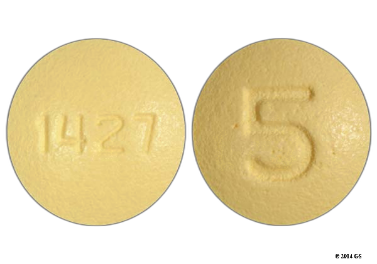
| Cảm quan | Viên nén tròn, bao phim màu vàng, hai mặt lồi, một mặt có khắc số “5”, một mặt khắc số “1427” | Viên nén hình thoi, bao phim màu vàng, hai mặt lồi, một mặt có khắc số “10”, một mặt khắc số “1428” |
 |
 |
|
| Kích thước | 7 mm | 11 x 8 mm |
| Tính chất cơ lý | 130 mg/ viên | 260 mg/ viên |
| Thành phần | Viên nhân
Bao phim:
|
Viên nhân
Bao phim:
|
| Quy trình bào chế | Xát hạt khô | Xát hạt khô |
| Bao bì | Bao bì cho cả 2 hàm lượng
EU: Hộp 1 vỉ x 14 viên, vỉ Al/Al (vỉ không đục lỗ) Hộp 2 vỉ x 14 viên, vỉ Al/Al (vỉ không đục lỗ) Hộp 7 vỉ x 14 viên, vỉ Al/Al (vỉ không đục lỗ) Hộp 1 vỉ x 30 viên, vỉ Al/Al (vỉ đục lỗ) Hộp 1 vỉ x 90 viên, vỉ Al/Al (vỉ đục lỗ) US: 1 chai (HDPE) x 30 viên 1 chai (HDPE) x 90 viên 1 chai (HDPE) x 500 viên Việt Nam: Hộp 2 vỉ x 14 viên, vỉ Al/Al |
|
| Hạn dùng | 36 tháng | |
| Doanh số | ~ 1,913 tỉ USD (2020) | |
| Pháp lý | Ngày đầu tiên được phê duyệt: 12/11/2012 (EU), 08/01/2014 (US)
Ngày hết patent: 04-10-2025 |
|
| Nước đã lưu hành: Châu Âu, Mỹ, Trung Quốc, Nhật Bản, Việt Nam… | ||
Patent tham khảo và hàm lượng tá dược trong thuốc gốc (chỉ dành cho tài khoản VIP)
Patent tham khảo: US 8,716,251 B2; US 8,361,972 B2; US 8,221,786 B2; US 7,851,502 B2
Hàm lượng tá dược trong thuốc gốc:
| Viên nén bao phim FORXIGA | 5 mg | 10 mg |
| Viên nhân | ||
| Microcrystalline cellulose | 85,725 | 171,45 |
| Lactose anhydrous | 25,00 | 50,00 |
| Crospovidone | 5,00 | 10,00 |
| Silicon dioxide | 1,875 | 3,75 |
| Magnesium stearate | 1,25 | 2,50 |
| Bao phim | ||
| Opadry II yellow chứa | 5,00 | 10,00 |
|
2,00
1,01 1,177 0,74 0,073 |
4,00
2,02 2,35 1,48 0,15 |
