Carbocistein
1. Thông tin chung
| Tên dược chất
Thông số |
Carbocistein | Carbocistein lysin monohydrat |
| Cấu trúc | 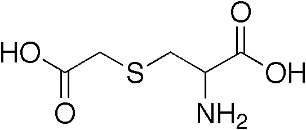 |
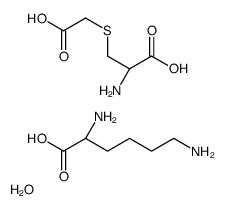 |
| Công thức phân tử | C5H9NO4S | C11H25N3O7S |
| KLPT | 179,2 | 343,4 |
| Hệ số chuyển đổi | NA | 1 g carbocistein lysin monohydrat tương ứng với 0,947 g carbocistein lysin |
| Nhóm tác dụng dược lý | Thuốc tiêu đờm – OTC | Thuốc tiêu đờm – OTC |
2. Biệt dược gốc và các dạng bào chế trên thị trường
Mục lục
2.1. Đơn chất
| STT | Dạng bào chế | Tên biệt dược |
| 1 | Viên nang cứng | Mucodyne, Rhinathiol |
| 2 | Sirô | Mucodyne, Rhinathiol |
| 3 | Bột pha dung dịch uống | Fluifort |
| 4 | Viên nén | Mucodyne |
Dạng bào chế phổ biến tại Việt Nam: Viên nang cứng, sirô, dung dịch uống, thuốc bột uống, viên nén, viên nén phân tán, viên nén sủi bọt
2.2. Dạng phối hợp
| STT | Hoạt chất | Dạng bào chế | Tên biệt dược |
| 1 | Promethazine hydrochlorid | Siro | Rhinathiol promethazine |
| 2 | Guafenesin | Siro | Tos Therapy Forte |
3. Tính chất lý hóa
| Carbocistein | Carbocistein lysin monohydrat | |
| Mô tả | Bột kết tinh màu trắng hoặc gần như trắng | NA |
| Tính tan | Thực tế không tan trong nước và cồn, tan được trong dung dịch acid vô cơ và base loãng | Tan tốt trong nước |
| Độ tan (thực nghiệm) | NA | NA |
| BCS Class | IV | NA |
| Nhiệt độ nóng chảy | 206oC | NA |
| Tính hút ẩm | NA | NA |
| pKa | 1,84 & 9,14 | NA |
| pH | 2,8 – 3,0 (lắc 0,2 g dược chất trong 20 ml nước đã loại CO2) | NA |
| Tính chất hóa học | Carbocistein có thể cho phản ứng đóng vòng cho carbocistein lactam (trong môi trường acid) hoặc bị oxy hoá tại lưu huỳnh cho sản phẩm carbocistein sulfoxid (gây thay đổi màu, mùi của hỗn hợp). | NA |
| Độ ổn định | Dược chất tương đối ổn định trong điều rắn.
Trong môi trường lỏng, dược chất kém ổn định hơn. Độ ổn định của thành phẩm phụ thuộc vào 1 số yếu tố như: pH dung dịch, thành phần dung dịch, bao bì bảo quản… |
NA |
4. Chuyên luận Dược Điển
| Monograph | Dược Điển |
| Carbocisteine | BP, EP, JP |
| Carbocistein Tablets | JP |
5. Nhà sản xuất API
- Moehs Catalana, SL (Spain)
- Wuhan Grand Hoyo Co., Ltd (China)
- Jizhou City Huayang Chemical Co., Ltd (China)
- Bretagne Chimie Fine (BCF) (France)
- PharmaZell (India) Private Limited (India)
6. Kinh nghiệm đối với hoạt chất – tương ứng với từng dạng bào chế
Chỉ dành cho tài khoản VIP
6.1. Kinh nghiệm thực tế:
- Những lưu ý khi xây dựng công với dạng lỏng (sirô hoặc dung dịch uống):
- Dược chất thực tế không tan trong nước, do vậy cần cho thành dạng muối dễ tan. Dung dịch carbocistein sau khi muối hoá có hơi có mùi, cân nhắc chọn nhưng chất tạo mùi mạnh để giúp thành phẩm có cảm quan tốt hơn
- Carbocistein sau một thời gian lưu độ ổn định không được ổn định, màu cũng có thể biến đổi nên cân nhắc các yếu tố như pH phù hợp sau khi muối hoá, chất tạo màu, tạo hương và chất chống oxi hoá
- Có thể cân nhắc sử dụng sodium CMC trong trường hợp không sử dụng đường nồng độ cao để tạo độ nhớt
6.2. Tài liệu cho xây dựng công thức:
- Patent WO 2014/096497 A [6]: Mô tả phương pháp bào chế dung dịch carbocistein gồm những thành phần: hoạt chất, ít nhất một chất điều chỉnh pH (có thể là monobasic sodium phosphat, dibasic sodium phosphat), một chất tạo mùi vị và dung môi nước.
- Patent FR9004470A [7]: Mô tả phương pháp bào chế sirô carbocistein gồm những thành phần: hoạt chất, đường, chất bảo quản. pH được điều chỉnh về khoảng 7,0 bằng sodium hydroxid.
Tài liệu tham khảo
-
- “Carbocysteine | C5H9NO4S – PubChem.” (accessed Jan. 14, 2022).
- “Carbocysteine lysine monohydrate | C11H25N3O7S – PubChem.” (accessed Jan. 14, 2022).
- “Carbocisteine EP10,” pp. 2084–2085.
- “Carbocisteine – BCS database.” (accessed Jan. 14, 2022).
- O. Wahl and U. Holzgrabe, “Impurity profiling of carbocisteine by HPLC-CAD, qNMR and UV/vis spectroscopy,” J. Pharm. Biomed. Anal., vol. 95, pp. 1–10, 2014, doi: 10.1016/J.JPBA.2014.02.012.
- “WO2014096497 PRÉPARATIONS LIQUIDES DE CARBOCISTÉINE À PROPRIÉTÉS AMÉLIORÉES.” (accessed Jan. 14, 2022).
- “FR2660553A1 – Syrup based on carbocisteine having improved stability – Google Patents.” (accessed Jan. 14, 2022).
