Brilinta (Ticagrelor)
 |
 |
 |
| Công ty sở hữu | AstraZeneca | ||
| API & liều dùng | Ticagrelor: 60, 90, 180 mg/ ngày | ||
| Hàm lượng | 60 mg | 90 mg | 90mg (ODT) |
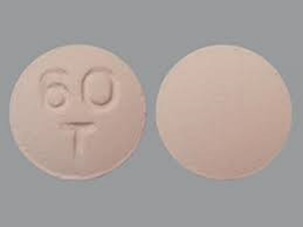
| Cảm quan | Viên nén bao phim, hình tròn, hai mặt lồi, màu hồng, một mặt khắc “60” và “T”, một mặt trơn. | Viên nén bao phim, hình tròn, hai mặt lồi, màu vàng, một mặt khắc “90” và “T”, một mặt trơn. | Viên nén tròn, phẳng, cạnh vát, màu trắng đến hơi hồng, một mặt khắc “90” và “TI”, một mặt trơn |
 |
 |
||
| Kích thước | 8,1 mm | 9,2 mm | – |
| Tính chất cơ lý | 207 mg/ viên | 309 mg/ viên | – |
| Thành phần |
|
|
|
| Quy trình bào chế | Xát hạt ướt | Xát hạt ướt | Xát hạt ướt |
| Bao bì (*) |
Hộp 4 vỉ x 14 viên, vỉ PVC-PVDC/Al |
Hộp 6 vỉ x 10 viên, vỉ PVC-PVDC/Al |
Hộp 1 vỉ x 10 viên, vỉ Al/Al |
| Hạn dùng | 36 tháng | 36 tháng | 36 tháng |
| Doanh số | – | ||
| Pháp lý | Ngày đầu tiên được phê duyệt: 07/20/2011
Ngày hết patent: N/A |
||
| Nước đã lưu hành: 39 nước trên thế giới bao gồm Mỹ, Canada, Bra-xin, Úc, Việt Nam và các nước khác trên thế giới. Tại Châu Âu, tên thương mại là Brilique | |||
(*) Còn 1 số quy cách đóng gói khác, tùy quốc gia
Patent tham khảo và hàm lượng tá dược trong thuốc gốc (chỉ dành cho tài khoản VIP)
Patent: US 8.425,934 B2
Hàm lượng tá dược trong thuốc gốc:
| Viên 60 mg | Viên 90 mg | |
| Viên nhân |
|
|
| Lớp bao phim |
|
|
