Aspirin
Mục lục
1. Thông tin chung
| Tên dược chất
Thông số |
Acetylsalicylic acid (aspirin) |
| Cấu trúc | 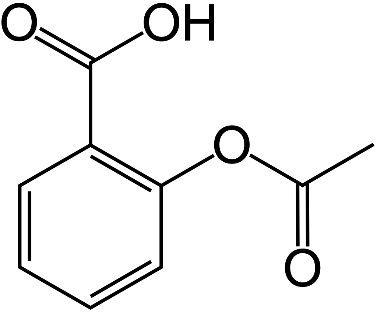 |
| Công thức phân tử | C9H8O4 |
| Số CAS | 50-78-2 |
| KLPT | 180.16 |
| Quy đổi | NA |
| Nhóm dược lý | Giảm đau hạ sốt
Chống kết tập tiểu cầu |
2. Biệt dược gốc và các dạng bào chế trên thị trường
2.1. Đơn chất
| STT | Dạng bào chế | Tên biệt dược |
| 1 | Viên nén | AspirinTM |
Dạng bào chế phổ biến tại Việt Nam: Viên nén bao phim, viên nén bao phim tan trong ruột, viên nén sủi bọt.
2.2. Dạng phối hợp
| STT | Hoạt chất phối hợp | Dạng bào chế | Tên biệt dược |
| 1 | Cafein | Viên nén | Anacin |
| 2 | Paracetamol, cafein | Viên nén | Anadin Extra
Excedrin |
| 3 | Codein | Viên nén | Co-codaprin |
| 4 | Dipyridamole | Viên nang GPKD | Aggrenox |
| 5 | Clopidogrel bisulfate | Viên nén bao phim | Duoplavin |
| 6 | Natri bicarbonat,
Acid Citric |
Viên nén sủi bọt | Alka-Seltzer |
3. Tính chất lý hóa
| Tên hoạt chất [1],[2] | Aspirin |
| Mô tả | Dạng tinh thể hoặc bột trắng, không mùi, vị hơi đắng |
| Tính tan | Ít tan trong nước. Tan tốt hơn trong ethanol (50 mg/mL) |
| Độ tan (thực nghiệm) | 2.5 g/L (15 °C) trong nước |
| BCS Class [3] | I |
| Nhiệt độ nóng chảy | 135 °C |
| Tính hút ẩm | Dễ hút ẩm, nhanh chóng bị thủy phân khi tiếp xúc với ẩm. |
| pKa | 3.5 |
| pH | 3.5 với dung dịch 2.5g/L tại 20 °C |
| Tính chất hóa học | Hơi acid nhẹ.
Bị thuỷ phân trong dung dịch nước hoặc môi trường có độ ẩm cao, tạo thành salicylic acid và acetic acid. |
| Độ ổn định | Ổn định trong điều kiện khô ráo.
Cần có biện pháp để tránh aspirin tiếp xúc với ẩm. |
4. Chuyên luận Dược Điển
| Monograph | Dược Điển (*) |
| Acetylsalicylic acid | EP |
| Acetylsalicylic acid tablets | WHO |
| Aspirin | USP, EP |
| Aspirin tablets | USP, BP |
| Aspirin boluses | USP |
| Aspirin capsule | USP |
| Aspirin Dispersible Tablets | BP |
| Aspirin Effervescent Soluble Tablets | BP |
| Aspirin Gastro-resistant Tablets | BP |
| Aspirin and Caffeine Tablets | BP |
| Co-codaprin Tablets | BP |
| Co-codaprin Dispersible Tablets | BP |
(*) Tài liệu chỉ tổng hợp 1 số chuyên luận chính, chi tiết các chuyên luận khác, vui lòng xem trong các dược điển USP, BP, EP.
5. Nhà sản xuất API
- Novacyl Limited (Thailand)
- JQC (Huayin) Pharmaceutical Co., Ltd (China)
- Dasan Pharmaceutical Co., Ltd (Korea)
6. Kinh nghiệm đối với hoạt chất – tương ứng với từng dạng bào chế
Chỉ dành cho tài khoản VIP
6.1. Kinh nghiệm thực tế:
Hoạt chất dất dễ bị thuỷ phân nếu gặp môi trường có độ ẩm cao, vì vậy cần tránh các kĩ thuật như xát hạt ướt bằng nước. Có thể sử dụng dung môi cồn để giảm thuỷ phân, hoặc sử dụng các biện phát dập trực tiếp, tạo hạt khô.
6.2. Tài liệu cho xây dựng công thức:
- Phát triển sản phẩm dạng dập trực tiếp[4]
- Patent EP2340814A2: Mô tả phương pháp bào chế viên nén chứa aspirin bằng phương pháp dập thẳng. Sau đó, viên được bao tan trong ruột sử dụng hệ bao chứa methacrylic acid-ethyl acrylate copolymer (1:1). Patent cũng nghiên cứu độ ổn định của công thức với 2 loại bao bì khác nhau và nhận thấy viên ép vỉ Al-PVC có độ ổn định kém hơn (viên bị mềm, xuất hiện tinh thể hình kim trên bề mặt) so với vỉ Al-Al.
Tài liệu tham khảo
[1] “Safety data sheet: Acetylsalicyclic acid.” Global Safety Management.[2] “Aspirin | HC9H7O4 – PubChem.” (accessed Feb. 24, 2022).
[3] J. B. Dressman et al., “Biowaiver monograph for immediate-release solid oral dosage forms: acetylsalicylic acid,” Journal of pharmaceutical sciences, vol. 101, no. 8, pp. 2653–2667, 2012, doi: 10.1002/JPS.23212.
[4] “EP2340814A3 – A stable aspirin tablet and process of preparation thereof – Google Patents.” (accessed Feb. 25, 2022).
